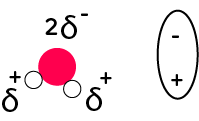Dissolution d'un cristal ionique
Que se passe-t-il lorsqu’on dissout un cristal ionique dans l’eau ?
Pour rappel, la molécule d’eau est une molécule polaire : au niveau de l’oxygène, il y a une zone avec une charge partielle négative et au niveau des hydrogènes, il y a une zone avec une charge partielle positive. On peut modéliser la molécule d’eau de la manière suivante :
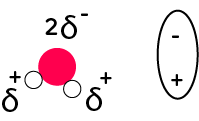
Une zone négative au niveau de l’oxygène et une zone positive au niveau des hydrogènes. Cela va nous aider à comprendre comment se passe la dissolution.
La dissolution se déroule en trois étapes : la dissociation, la solvatation et la dispersion.
La dissociation
Lors de la dissociation, les molécules d’eau s’approchent des ions du cristal ionique, qui est ici le cristal de sel composé d’une alternance d’ions Chlorure (Cl-) et d’ions Sodium (Na+). Lorsque la molécule d’eau s’approche de l’ion chlorure, elle va présenter le côté où il y a les hydrogènes, c’est le côté positif, et éloigner le côté où il y a l’oxygène puisque c’est le côté négatif. L’ion chlorure va être attiré par la molécule d’eau. Par contre, cela va être l’inverse pour l’ion sodium. La molécule d’eau va s’approcher du côté de l’oxygène qui est une zone négative et mettre à l’opposé les hydrogènes puisque c’est le côté positif. De cette manière, l’ion sodium va être attiré par la molécule d’eau. Progressivement, les molécules d’eau attirent les ions et dissocient le cristal ionique.
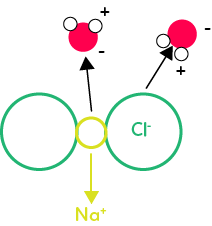
La solvatation
Dans ce phénomène, les molécules d’eau vont entourer les ions après les avoir disloqués du cristal ionique. Les molécules d’eau vont se disposer autour de l’ion chlorure de la manière suivante, puisqu’ici on a les zones positives de la molécule d’eau et à l’opposé la zone négative de la molécule d’eau :
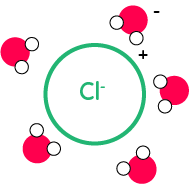
Pour l’ion sodium, c'est l’inverse. Les molécules d’eau vont se disposer autour de l’ion de la manière suivante, puisqu’au niveau de l’oxygène on a une partie négative et une partie positive au niveau des hydrogènes :
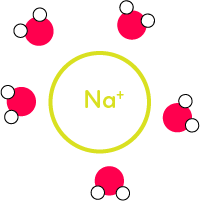
La dispersion
Tout se mélange de façon homogène dans l’espace. La dissolution est évidemment favorisée par l’agitation, qui va permettre d’accélérer ce phénomène de dispersion et d’avoir une solution bien homogène.
Équation bilan
L’équation bilan de la réaction, dans le cas du chlorure de sodium ou sel de table, s'écrit de la manière suivante :
$NaCl (s) \rightarrow Na^+ (aq) + Cl^- (aq)$
NaCl, la formule du cristal de sel, donne Na+ et Cl-. On ne fait pas figurer l’eau car elle est toujours présente dans cette dissolution. On indique juste que NaCl, le cristal ionique, se dissocie en ions Na+ solvatés (aqueux), et en ions Cl- solvatés (aqueux).
Voyons maintenant le cas d’un cristal où il n’y a pas seulement un anion et un cation mais où il y a un cation et deux anions : le cristal de formule CaF2. Il va donner un ion Ca2+ (aq) et deux ions fluorure F-(aq).
$CaF_2 (s) \rightarrow Ca^{2+} (aq) + F^-(aq)$
Effectivement, dans la formule du cristal on a deux F- pour un Ca2+ donc on va retrouver le nombre stœchiométrique « 2 » au niveau de l’équation de dissolution. Cela va avoir une conséquence au niveau des concentrations.
Concentration
Effectivement, on a la concentration en soluté apporté notée CCaF2 , c’est le nombre de moles de soluté divisé par le volume de la solution :
$C_{CaF_2}= \dfrac{n_{ CaF_2}}{V_{sol}}$
Elle ne va pas être égale, dans tous les cas, à la concentration en ions réelle présents dans la solution. En effet, quand on dissout un cristal ionique CaF2 on a un ion Ca2+ mais on a deux ions F-. En fait, la concentration en ion Ca2+ va être égale à la concentration CCaF2 :
$[Ca^2+]= \dfrac{n_{Ca^2+}}{V_{sol}} = C_{CaF_2}$
Par contre, on a deux fois plus d’ions F- que de cristaux de CaF2 :
$[F^-]= \dfrac{n_{F^-}}{V_{sol}} = 2 C_{CaF_2}$