Description d'un fluide au repos
I. Description du fluide
Vision microscopique
Microscopiquement, un fluide peut être un liquide ou un gaz composé de particules (molécules ou atomes par exemple). Donc, quelle est la différence entre un liquide et un gaz ?
- Dans un liquide, les particules sont assez proches les unes des autres, quasiment en contact, car il y a des interactions fortes.
- Dans un gaz, les particules sont éloignées et il y a peu d’interactions entre les particules, voir aucune, dans le cas des gaz parfaits.
Dans tous les cas, que ce soit liquide ou gaz, il y a beaucoup de particules (molécules et atomes) dans un système considéré, même dans 1 ml d’eau. Si on veut décrire ce qui se passe en indiquant, par exemple, la vitesse et la position de chacune des particules, il y aura une quantité d’informations beaucoup trop importante pour décrire un fluide. Donc, la vision microscopique est intéressante mais extrêmement complexe, c’est pourquoi on passe à une vision macroscopique pour voir les choses de plus loin.
Vision macroscopique

On va tenter de caractériser ces quelques gouttes d'eau et de trouver des paramètres dans son ensemble. Ces paramètres sont par exemple son volume, sa température, sa pression et $N$ la quantité de particules à l’intérieur. C’est ce qu’on appelle des grandeurs macroscopiques, c’est-à-dire qu’elles décrivent un ensemble de particules et non pas une seule.
Pour le volume on utilise le mètre cube qui est l’unité internationale ; pour la température, le kelvin ; pour la pression, le pascal et le nombre de particules est sans unité.
II. La pression
Quand on gonfle un pneu d’air, on se rend compte que la pression augmente quand on injecte de l’air. On fait rentrer des molécules dans un espace confiné et on constate que ça « pousse ».
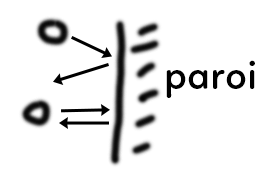
Sur le schéma, on voit une paroi à droite et des particules (molécules) agitées dans le fluide, quand elles arrivent sur la paroi, elles tapent puis repartent. Dans certains modèles, qu’on appelle modèles élastiques, on considère un peu comme au billard, que la particule va venir taper et repartir, notamment avec le même angle d’incidence. Mais en faisant ceci, elle a transféré une quantité de mouvement.
On voit qu’il y a une pression transférée sur la paroi. La pression est donc liée à la collision des particules de fluide sur la paroi. Plus il y en a, plus la pression est importante. On comprend donc que plus on injecte de particules, plus la pression est importante.
L’unité est le pascal (Pa).
Il faut s’habituer à faire des conversions, car dans un grand nombre d’exercices, les données ne seront pas données en Pascal :
1 hectopascal donne 100 pascal,
1 bar équivaut à 105 pascal (100 000 pascal),
1 atmosphère c’est 1 013,25 hectopascal (101 325 pascal). C’est en quelque sorte, la pression moyenne sur Terre.
III. La température
La température mesure l’agitation des molécules. Plus la température augmente, plus les molécules sont agitées, c’est-à-dire que leur vitesse augmente.
L’unité de la température dans le système international est le kelvin et non le degré Celsius. On sait que la température en Kelvin est la température en degrés Celsius $+ 273,15.$
$T(K) = T(°C) + 273,15$
Le degré Celsius a été introduit car il était utilisé pour des points précis comme 0°C qui correspond au point de solidification de l’eau, ou encore 100°C qui est la température d’ébullition à pression atmosphérique.
La température en Kelvin a-t-elle une signification, un point précis comme le degré ? Oui, car comme dit auparavant, l’agitation c’est ce qui mesure la température, et à 0 Kelvin il n’y a pas d’agitation. On peut le retrouver notamment dans les laboratoires de recherche : à l’heure actuelle, il y a des scientifiques qui essayent de diminuer le plus possible l’agitation des molécules pour essayer d’atteindre le 0 Kelvin. Le 0 Kelvin précisément, n’a toujours pas été atteint.