Changements d'états
I. Quels sont les changements d'états existants ?
La matière existe à l’état solide, liquide ainsi que gazeux. Les changements entre ces différents états on des noms qu’il faut connaître :
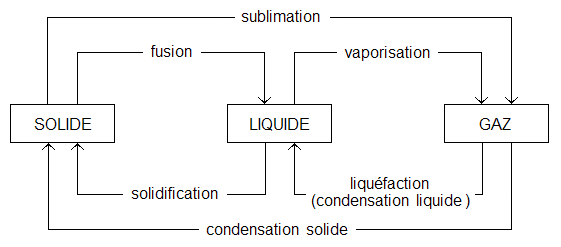
Le changement d’état du solide vers le liquide est la fusion.
Le changement d’état du liquide vers le solide est la solidification.
Le changement d’état du liquide vers le gaz est la vaporisation.
Le changement d’état du gaz vers le liquide est la liquéfaction.
Le changement d’état du solide vers le gaz est la sublimation.
Le changement d’état du gaz vers le solide est la condensation.
Lorsque l’on veut écrire l’équation d’un changement d’état (fusion) pour un corps pur, par exemple de l’eau, il suffit d’écrire :
$H_2 O_{(s)} \to H_2 O_{(l)} $
II. Changements d'états endothermiques et exothermiques
D’un point de vue énergétique, certains changements d’états sont endothermiques et d’autre exothermiques :
- Un changement d’état est dit endothermique lorsque l’on doit apporter de l’énergie à la réaction. Les changements concernés sont la sublimation, la fusion et et la vaporisation
- A l’opposé un changement d’état est exothermique lorsqu’il dégage de l’énergie, cela concerne la liquéfaction, la solidification et la condensation.
III. Energie de changement d'état Q
Il existe une énergie de changement d’état notée Q qui peut se déterminer.
La formule à connaître est $Q =m \times L,$ où $Q$ s'exprime en joules (J), la masse en kilogrammes (kg) et l'énergie massique, que l'on note $L,$ en joules par kilogramme (J.kg-1).
Toutes les énergies massiques de changements d’états sont répertoriées dans une base de donnée accessible (un livre).
Exemple : la fusion de l’eau
Son énergie massique de changement d’état est $L_{fusion}(H_2O)=330 \ kJ.kg^{-1}$.
Ainsi pour faire fondre $1 \ kg$ de glace, il faut fournir $330 \ kJ$. De plus, par convention, un changement d’état endothermique possède une énergie Q positive, et pour un changement d’état exothermique Q est négative.
Pour finir, lorsque que deux changements d’états sont opposés l’un à l’autre, alors leur énergie massique de changement d’états sont opposées : $L_{fusion}=-L_{solidification}$ et $L_{vaporisation}=-L_{liquéfaction}$.