Le modèle de l'atome
I. Modèle
Un atome est une entité neutre (ce n’est pas un ion !).
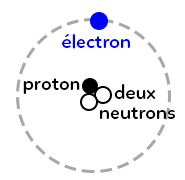
Un atome est composé d’un noyau, qui lui même est composé de neutrons et de protons ainsi que d’électrons qui gravitent autour du noyau.
On appelle aussi les neutrons et les protons des nucléons.
Charges
Les électrons sont chargés négativement, les protons sont chargés positivement.
Les neutrons n’ont pas de charges.
Comme un atome est une entité neutre, cela veut dire qu’il y a toujours le même nombre de protons et d’électrons pour un atome.
Masse
On considère que la masse de l’atome est environ la même que la masse du noyau de l’atome. En effet, les électrons sont extrêmement légers par rapport aux nucléons.
Une formule assez naïve est : $m_{noyau}=A \times m_{nucléon}$, où $A$ est le nombre de nucléons dans le noyau.
II. Notation
Il y a une notation spécifique aux atomes qu’il faut connaître. On les note : $^{A}_{Z}X$, où $X$ est le symbole de l’élément, $A$ est le nombre de nucléons et $Z$ est le nombre de protons appelé le numéro atomique.
Pour trouver le nombre de neutrons la formule est donc : $N=A-Z$.
Exemple : l’hydrogène se note : $^{1}_{1}H.$ Celui-ci possède donc 1 nucléon (A=1) et 1 proton (Z=1), donc il ne possède pas de neutrons.
III. Répartition des électrons en couche
Les électrons se répartissent sous forme de couches autour du noyau :
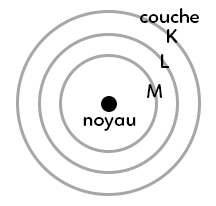
La première couche est la couche (K), la deuxième (L) et la troisième (M). Les électrons vont se répartir selon leur nombre sur les différentes couches en commençant par la couche intérieure (K). Néanmoins, chaque couche possède un nombre maximal d’électrons qu’elle peut contenir :
K : 2 électrons maximum
L : 8 électrons maximum
M : 18 électrons maximum
On remplit ensuite d’abord K, puis L, puis M.
Exemple : l’atome de carbone se note $^{12}_{6}C.$ Il y a donc 6 protons dans le noyau, ce qui veut dire qu’il y a 6 électrons à placer sur les couches. En effet, l’atome doit rester neutre. La répartition est donc $(K)^2 (L)^4.$