Faire un dosage par étalonnage nécessite de faire une mesure indirecte, non destructible, en utilisant et en mesurant différentes grandeurs. On étudie deux types de dosage par étalonnage : le dosage à l’aide d’un spectrophotomètre et le dosage à l’aide d’un conductimètre.
Dosage à l’aide d’un spectrophotomètre
Pour le dosage à l’aide d’un spectrophotomètre, la grandeur mesurée par celui-ci est l’absorbance $A.$ L’absorbance $A$ est définie par la loi de Beer-Lambert. L’absorbance est proportionnelle à la concentration : $A = k\times C$.
Le coefficient de proportionnalité dépend de plusieurs choses : types de spectrophotomètre, longueur de la cuve, etc. L’absorbance est sans unité, la concentration est en mol.L-1.
Comment dose-t-on une solution, par étalonnage, à l’aide de l’absorbance ?
Si on trace l’absorbance en fonction de la concentration, comme c’est proportionnel on a une droite qui passe par l’origine.
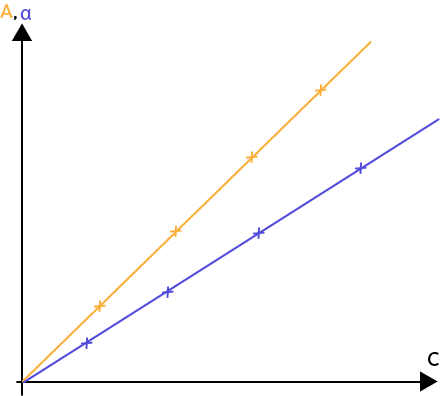
Si la concentration est égale à zéro, l’absorbance aussi. Il faut mesurer l’absorbance d’un certain nombre de solutions connues, dont on connaît la concentration. On mesure ensuite l’absorbance de cette solution inconnue, et, grâce à une droite d’étalonnage, par correspondance, on peut trouver la concentration de la solution inconnue.
Dosage à l’aide d’un conductimètre
On utilise un conductimètre pour mesurer la conductivité $σ$ définie par la loi de Kohlrausch : $ σ = k\times C$ qui est aussi une loi de proportionnalité. Si on trace $σ$ en fonction de la concentration, on a aussi une droite qui passe par l’origine. Si on veut connaître la concentration d’une solution inconnue, on mesure la conductivité $σ$ et on peut en déduire, par rapport à la droite d’étalonnage, la concentration de la solution inconnue.
Quelles sont les limites ?
Les limites, dans les deux cas, sont que cela ne fonctionne pas pour des solutions trop concentrées. Si la solution est trop concentrée, l’absorbance va être trop forte et le spectrophotomètre ne va pas pouvoir capter assez de lumière. Cela pose des problèmes. Il en va de même pour la conductivité et la concentration.
Pour le conductimètre, s’il y a d’autres ions qui sont présents dans le milieu, cela peut fausser la conductivité. Un des paramètres importants pour le spectrophotomètre, est de savoir à quelle longueur d’onde on se place pour régler le spectrophotomètre, pour mesurer l’absorbance. On se place toujours au maximum d’absorbance de la solution. Si on trace le graphe de l’absorbance de la solution en fonction de la longueur d’onde, l’absorbance de la solution va varier en fonction de la longueur d’onde.
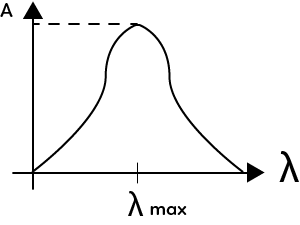
Il faut donc se mettre à la longueur d’onde $λ_{max}$ pour une absorbance maximale.
Les applications de ces deux types de dosages
On peut demander d’utiliser ces droites d’étalonnage en utilisant l’absorbance ou la conductivité et de retrouver la concentration. On peut aussi demander de réfléchir sur les paramètres importants : la longueur d’onde choisie pour l’absorbance, les ions qui vont fausser la conductivité. Ce qui est important, ce sont également les capacités expérimentales. On peut demander de réfléchir sur un protocole où l’on va utiliser soit le spectrophotomètre soit le conductimètre.