Terminale > Physique-Chimie > Constitution et transformations de la matière > Stage - La pile
- Mesure et incertitudes
-
Constitution et transformations de la matière
- Exercices corrigés en vidéo : Modéliser des transformations acide-base
- Exercices corrigés en vidéo : Analyse physique d'un système chimique
- Exercices corrigés en vidéo : Évolution temporelle d'une transformation chimique
- Couple acide-base et réaction
- pH et relation
- Absorbance, conductance, conductivité
- Analyse spectrale
- Titre massique, titrages
- Cinétique, catalyse et vitesse de réaction
- Réactions nucléaires et radioactivité
- Équilibre chimique
- La pile
- Oxydant, réducteur et équation d'oxydoréduction
- Comparer la force des acides et des bases
- Électrolyse
- Formule topologique et isomères
- Polymérisation
- Stage - Couple acide-base et réaction
- Stage - pH et relation ; absorbance ; conductance, conductivité
- Stage - Analyse spectrale
- Stage - Titre massique, titrages
- Stage - Cinétique, catalyse et vitesse de réaction
- Stage - Réactions nucléaires et radioactivité
- Stage - Équilibre chimique
- Stage - La pile
- Stage - Oxydant, réducteur et équation d'oxydoréduction
- Stage - Comparer la force des acides et des bases
- Stage - Formule topologique, isomère, polymérisation
- Stage - Exercices corrigés en vidéo
-
Mouvement et interactions
- Exercices corrigés en vidéo
- Décrire un mouvement
- Référentiel galiléen et deuxième loi de Newton
- Mouvement dans un champ de pesanteur uniforme
- Système dans un champ électrique, accélérateur linéaire de particules
- Mouvement d'un satellite autour d'une planète
- Chute d'un objet sans vitesse
- Chute d'un objet avec vitesse
- Poussée d'Archimède, écoulement d'un fluide
- Relation de Bernoulli, effet Venturi
- Stage - Décrire un mouvement
- Stage - Référentiel galiléen et deuxième loi de Newton
- Stage - Mouvement dans un champ de pesanteur uniforme
- Stage - Système dans un champ électrique, accélérateur linéaire de particules
- Stage - Mouvement d'un satellite autour d'une planète
- Stage - Chute d'un objet sans vitesse
- Stage - Chute d'un objet avec vitesse
- Stage - Poussée d'Archimède, écoulement d'un fluide
- Stage - Relation de Bernoulli, effet Venturi
-
L’énergie : conversions et transferts
- Exercices corrigés en vidéo
- Modèle du gaz parfait
- Système et énergie interne U
- Premier principe de la thermodynamique
- Énergie interne d'un système incompressible
- Transferts thermiques
- Bilan énergétique
- Flux thermique : résistance, thermostat
- Bilan thermique du système Terre-atmosphère
- Stage - Modèle du gaz parfait
- Stage - Système, transferts thermiques
- Stage - Premier principe de la thermodynamique
- Stage - Énergie interne d'un système incompressible
- Stage - Bilan énergétique
- Stage - Flux thermique : résistance, thermostat
- Stage - Bilan thermique du système Terre-atmosphère
-
Ondes et signaux
- Exercices corrigés en vidéo
- Diffraction et interférences
- Intensité sonore et atténuation
- L'effet Doppler
- Lunette astronomique et grossissement
- L’effet photoélectrique
- Rendement d'une cellule photovoltaïque
- Charge et décharge d’un condensateur
- Stage - Intensité sonore et atténuation
- Stage - Diffraction et interférences
- Stage - Effet Doppler
- Stage - Lunette astronomique et grossissement
- Stage - L’effet photoélectrique
- Stage - Rendement d'une cellule photovoltaïque
- Stage - Charge et décharge d’un condensateur
- Méthodologie et ECE
- Stage de pré-rentrée Physique-Chimie Terminale
STAGE - LA PILE
Accède gratuitement à cette vidéo pendant 7 jours
Profite de ce cours et de tout le programme de ta classe avec l'essai gratuit de 7 jours !
Fonctionnement d'une pile
Permalien- Exercices corrigés en vidéo : Modéliser des transformations acide-base
- Exercices corrigés en vidéo : Analyse physique d'un système chimique
- Exercices corrigés en vidéo : Évolution temporelle d'une transformation chimique
- Couple acide-base et réaction
- pH et relation
- Absorbance, conductance, conductivité
- Analyse spectrale
- Titre massique, titrages
- Cinétique, catalyse et vitesse de réaction
- Réactions nucléaires et radioactivité
- Équilibre chimique
- La pile
- Oxydant, réducteur et équation d'oxydoréduction
- Comparer la force des acides et des bases
- Électrolyse
- Formule topologique et isomères
- Polymérisation
- Annale - Hydratation lors d'un marathon
- Annale - Vitamine C
- Annale - Crème anesthésiante
- Annale - Eliminer le tartre
- Stage - Couple acide-base et réaction
- Stage - pH et relation ; absorbance ; conductance, conductivité
- Stage - Analyse spectrale
- Stage - Titre massique, titrages
- Stage - Cinétique, catalyse et vitesse de réaction
- Stage - Réactions nucléaires et radioactivité
- Stage - Équilibre chimique
- Stage - La pile
- Stage - Oxydant, réducteur et équation d'oxydoréduction
- Stage - Comparer la force des acides et des bases
- Stage - Formule topologique, isomère, polymérisation
- Stage - Exercices corrigés en vidéo
4 éléments
Fonctionnement d'une pile
Une pile est un objet qui convertit l’énergie chimique en énergie électrique avec quelques pertes sous forme d’énergie thermique. Précisons qu’une pile et un accumulateur ont le même fonctionnement, la seule différence c’est qu’un accumulateur peut être rechargé alors qu’une pile, par définition, ne peut pas être rechargée.
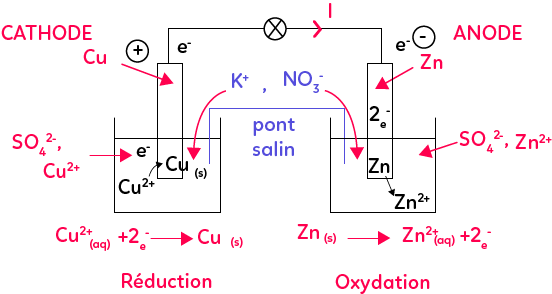
I. Constitution d'une pile
Une pile est constituée de deux demi-piles (gauche et droite) reliée par un pont salin. La pile que l’on étudie ici est la pile Daniell. Chaque demi-pile est constituée par une électrode qui est le plus souvent un métal et qui plonge dans une solution conduisant l’électricité donc une solution qui contient des ions.
La première demi-pile est constituée d’une lame de Cuivre plongée dans une solution de sulfate de Cuivre composée d’ions sulfate SO42- et des ions Cuivre Cu2+.
La deuxième demi-pile est constituée d’une lame de Zinc qui trempe dans une solution contenant du sulfate de Zinc (SO42- et Zn2+).
II. Fonctionnement d'une pile
On fournit ici les deux demi-équations d’oxydo-réduction qui permettent d’expliquer le fonctionnement de cette pile puisque c’est effectivement une réaction d’oxydo-réduction qui est à l’origine du fonctionnement de la pile.
Le métal Zinc va se transformer en Zn2+ en « éjectant » deux électrons. Les deux électrons vont partir de l’électrode de Zinc, vont arriver au niveau du circuit par le fil conducteur et vont traverser le récepteur branché aux bornes de la pile pour arriver ensuite de l’autre côté. En arrivant de l’autre côté, les électrons vont être captés par le Cu2+ en solution pour former du Cuivre solide grâce aux électrons. C’est cet échange d’électrons dans les réactions d’oxydo-réduction qui est à l’origine du courant électrique puisque, les électrons, en passant d’une demi-pile à une autre, vont donc produire ce courant électrique qui va faire fonctionner le récepteur, comme la lampe.
III. Bornes d'une pile
Voyons maintenant comment trouver les bornes de la pile. Si les électrons partent de l’électrode de Zinc pour aller vers celle de Cuivre, alors le Zinc sera la borne « - » (deux charges « - » se repoussent) et le Cuivre la borne « + » (les électrons chargés négativement vont être attirés par la borne « + »).
Par définition, l’électrode où se passe l’oxydation est appelée anode et celle où il y a une réduction est appelée cathode (moyen mnémotechnique : anode et oxydation = voyelles ; cathode et réduction = consonnes).
La demi-équation du Zinc est celle qui correspond à une oxydation puisqu’on forme ici l’oxydant. L’électrode de Zinc est alors l’anode. La demi-équation du Cuivre est celle qui correspond à une réduction puisqu’on forme le réducteur du couple. Cette électrode sera appelée la cathode. Dans le cas d’une pile, l’anode est toujours négative et la cathode est positive mais ça n’est pas toujours le cas donc il faut toujours bien le démontrer.
IV. Sens conventionnel du courant électrique
Une fois que l’on a le sens de déplacement des électrons qui est indiqué, on peut avoir le sens conventionnel du courant électrique. Le sens du courant électrique c’est l’opposé de celui des électrons. Il est orienté dans le sens inverse ce qui est logique puisqu’on sait que le courant électrique va de la borne « + » de la pile vers la borne « - » de la pile, en passant par l’extérieur du circuit.
V. Importance du pont salin
Il ne faut pas oublier le pont salin dans les expériences. Généralement, en TP, si la pile de fonctionne pas, c’est que le pont salin a été oublié. Le pont salin est un papier filtre ou du gel qui contient des ions à l’intérieur. Il permet de faire la jonction au niveau des solutions de la pile et il assure l’électroneutralité de la pile. En effet avec la réaction du Zinc, on produit des ions Zn2+, on a donc des charges positives qui arrivent dans la solution.
Une solution ne peut pas être chargée positivement, elle est toujours neutre. On a les ions NO3- qui vont venir dans la solution de sulfate de Zinc pour compenser les charges positives qui apparaissent. A l’inverse, de l’autre côté, on va consommer des charges positives, on va avoir plus de SO42- que de Cu2+. Pour compenser cette charge positive qui disparaît de la solution, on va avoir des ions K+ du pont salin qui vont arriver dans la solution de sulfate de Cuivre.
VI. Quand la pile arrête-t-elle de débiter ?
Elle s’arrête de débiter lorsqu’il n’y a plus d’électrode de Zinc, ce qui n'est pas souvent le cas, ou lorsqu’il n’y a plus de Cu2+. C’est souvent le Cu2+ qui limite le fonctionnement de la pile. On va donc écrire l’équation d’oxydo-réduction qui régit le fonctionnement de cette pile. Il suffit d’additionner ces deux demi-équations d’oxydo-réduction.
Cette fiche de cours est réservée uniquement à nos abonnés. N'attends pas pour en profiter, abonne-toi sur lesbonsprofs.com. Tu pourras en plus accéder à l'intégralité des rappels de cours en vidéo ainsi qu'à des QCM et des exercices d'entraînement avec corrigé en texte et en vidéo.