Une enzyme est une protéine qui joue le rôle de biocatalyseur, in vivo elle va catalyser, faciliter des réactions biochimiques. Pour cela, elle va agir sur une molécule en particulier : son substrat.
Comment se déroule la catalyse enzymatique ?
Ce mode d’action a été étudié par deux scientifiques : Michaelis et Menten, au début du XXe siècle. Mais, auparavant, un autre scientifique nommé Fisher avait déjà une intuition sur une complémentarité des formes de l’enzyme et de son substrat et donc un attachement possible (une fixation transitoire) qui aurait rendu possible cette catalyse enzymatique.
Une enzyme est une protéine donc elle est produite par l’expression d’un ou plusieurs gènes. C’est une suite d’acides aminés attachés les uns aux autres par des liaisons peptidiques. Comme toutes les protéines, grâce à ses acides aminés, l’enzyme va avoir de façon native une configuration tridimensionnelle particulière. On a donc une forme particulière que prennent les acides aminés de façon naturelle au moment de la production de l’enzyme. Cette forme spécifique va délimiter ce qu’on appelle un site actif pour l’enzyme. C’est un ensemble de quelques acides aminés, en général une dizaine voire parfois une centaine, qui va comprendre un site de liaison au substrat et également un site catalytique (par exemple : couper un substrat en deux ou en attacher deux ensemble pour en faire un autre particulier). Cette enzyme, grâce à son site actif, va se lier à son substrat. On va pouvoir décrire comme un cycle de catalyse, représenté ici.
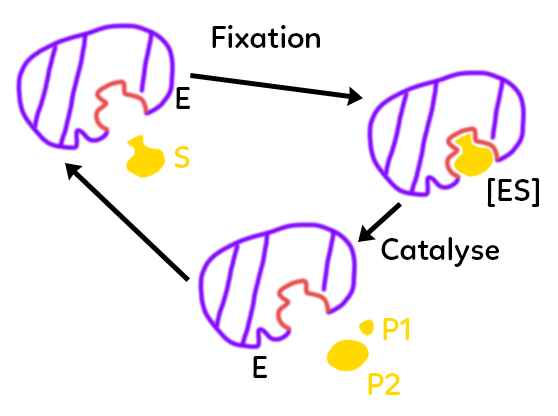
L’enzyme (violet) au départ présente un site actif (rouge) qui comprend à la fois le site de liaison et le site catalytique. Le substrat (jaune) va pouvoir, grâce à sa forme, être adapté à la forme du site actif. Ils vont donc se lier et former un complexe enzyme-substrat [ES].
Au départ pour Fisher, le modèle était plutôt rigide et le substrat s’adaptait à l’enzyme comme une clé dans une serrure. En réalité, actuellement, on pense plutôt qu’il y a une adaptation, un ajustement induit.
Les formes de l’enzyme et du substrat sont complémentaires mais peuvent être légèrement modifiées au moment où le complexe se forme. Lorsque le complexe enzyme-substrat est formé, le rôle catalytique de l’enzyme va pouvoir se jouer : les acides aminés partie catalytique du site vont faciliter la découpe en deux du substrat. On va avoir la catalyse et la division du substrat en deux produits P1 et P2. Ces deux produits quittent ensuite le site actif qui est libéré et l’enzyme est récupérée telle quelle dans sa forme initiale. On retourne donc à l’état initial avec possibilité pour l’enzyme de servir à nouveau.
On obtient cette réaction : E+S -> [ES] -> E+P
La présence du site actif avec sa forme particulière due à la composition en acides aminés est responsable de deux caractéristiques des enzymes :
- La spécificité du substrat : grâce à sa forme. Par exemple, on a vu que l’amylase de notre salive est une enzyme adaptée pour l’hydrolyse de l’amidon. Si on met cette enzyme en présence d’un autre glucide, la cellulose, dont la formule est proche mais pas tout à fait identique à celle de l’amidon alors l’amylase n’est pas efficace pour hydrolyser la cellulose.
- La spécificité d’action : grâce aux acides aminés de la partie catalytique. En effet, une enzyme va avoir qu’une action biochimique particulière. Par exemple, ici, elle coupe le substrat en deux produits. Il existe des enzymes qui ont d’autres modes d’action : attacher deux substrats en un seul produit.
Il y a donc une double spécificité des enzymes et cela est dû à la présence du site actif aménagé en fonction de sa composition en acides aminés dans la protéine. L’enzyme revient à son état initial et peut être réutilisée à l’infini. Néanmoins, l’enzyme comme toute protéine est dénaturable. Par exemple, sous une trop forte chaleur. Si on place de l’amylase à une plus grande température que celle du corps humain, l’enzyme va être dénaturée. C’est-à-dire que la structure tridimensionnelle totale de la protéine est désorganisée et on perd le site actif : l’enzyme ne peut plus agir.
Chaque enzyme a un pH optimal, si on modifie ce pH (par exemple : pH acide), la structure tridimensionnelle de l’enzyme sera perdue et le site actif n’existe plus : l’enzyme est dénaturée. Enfin, on comprend aussi qu’une mutation génétique qui modifierait la séquence d’acides aminés pourrait avoir des conséquence sur la forme de l’enzyme et rendre l’enzyme inutilisable, ce qui est parfois source de maladies génétiques.
 Mode d'action de la catalyse enzymatique
Mode d'action de la catalyse enzymatique
 QCM - Mode d’action de la catalyse enzymatique
QCM - Mode d’action de la catalyse enzymatique
 QCM - La catalyse enzymatique
QCM - La catalyse enzymatique
 Étude de la cinétique de l'activité catalytique enzymatique
Étude de la cinétique de l'activité catalytique enzymatique
 QCM - Cinétique de l'activité catalytique enzymatique
QCM - Cinétique de l'activité catalytique enzymatique
 Exercice - Étude de la cinétique de l'activité enzymatique
Exercice - Étude de la cinétique de l'activité enzymatique


