Il existe des solutions aqueuses acides, basiques ou neutres. Pour savoir si une solution est acide, basique ou neutre, on mesure le pH. Pour mesurer le pH, il y a deux possibilités :
- Déposer une goutte sur le papier pH à l’aide d’une pipette, et ensuite comparer la couleur du papier pH avec le code couleur qui attribue une valeur du pH à chaque couleur.
- Utiliser un pH-mètre, plus précis. On le plonge directement dans la solution à tester et le pH apparaît sur le cadran numérique.
Si le pH est inférieur à 7, la solution est acide.
Si le pH est égal à 7, la solution est neutre.
Si le pH est supérieur à 7, la solution est basique.
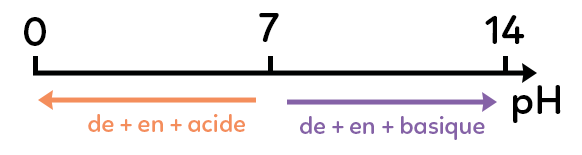
Sur l’échelle de pH représentée ci-dessus les solutions neutres sont situées à 7. Le pH va de 0 à 14.
Plus le pH est petit, plus il va vers 0 et plus la solution est acide.
Plus le pH est grand, de 7 à 14, plus la solution est basique.
Quelle est la composition de ces solutions acides et basiques en termes d’ions ?
Nous étudions l’ion hydrogène H+ et l’ion hydroxyde HO-.
Dans une solution acide, il y a plus d’ions hydrogène H+ que d’ions hydroxyde HO-.
Dans une solution neutre, il y a autant d’ions hydrogène H+ que d’ions hydroxyde HO-.
Dans une solution basique, c’est l’inverse que pour une solution acide, il y a plus d’ions hydroxyde HO- que d’ions hydrogène H+.
Réactions entre les acides et les bases
Si on a une solution acide et qu’on lui rajoute une solution basique, le pH augmente pour atteindre la neutralité (pH = 7).
Si on a une solution basique et qu’on y rajoute une solution acide, le pH diminue de manière à tendre vers la neutralité (pH = 7).
Les réactions entre acides et bases peuvent s’écrire de la manière suivante : H+ + HO- → H2O.
C’est une réaction entre H+ qui est caractéristique de l’acidité et HO- une caractéristique de la basicité.




