Troisième > Mission Brevet Physique-Chimie > Mes sujets de brevet > Organisation et transformation de la matière
ORGANISATION ET TRANSFORMATION DE LA MATIÈRE
Exercice d'application
Organisation et transformation de la matière
-
L'acide acétylsalicylique est plus connu sous le nom d'aspirine. C’est la substance active de nombreux médicaments utilisés dans les traitements de la douleur (antalgique), de la fièvre (antipyrétique) et des inflammations (anti-inflammatoire). En France, plus de 200 médicaments commercialisés contiennent de l'aspirine.
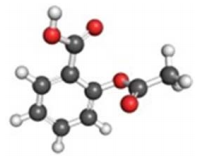
Formule de l’aspirine : $C_9H_8O_4$
Question 1 : Indiquer le nombre d’atomes d’oxygène présents dans la molécule d’aspirine.
Question 2 : Pour certains traitements médicaux particuliers, le médecin prescrit des gélules d’aspirine gastrorésistantes afin que l’absorption de la substance active se fasse au niveau de l’intestin plutôt qu’au niveau de l’estomac. Comme leur nom l’indique, les gélules gastrorésistantes résistent à l’acidité de l’estomac, dite acidité gastrique, grâce à la pellicule spécifique dont elles sont enrobées.
Document 1 : système digestif
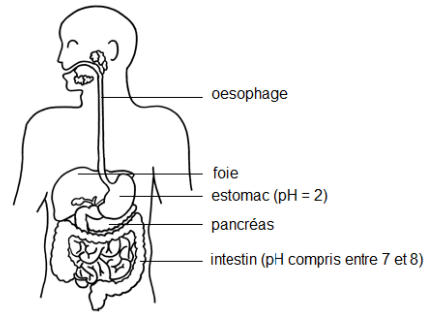
En exploitant le document 1, proposer un protocole expérimental permettant de prouver qu’une gélule d’aspirine gastrorésistante résiste à l’acidité gastrique. On pourra formuler la réponse sous forme de texte et/ou de schémas.
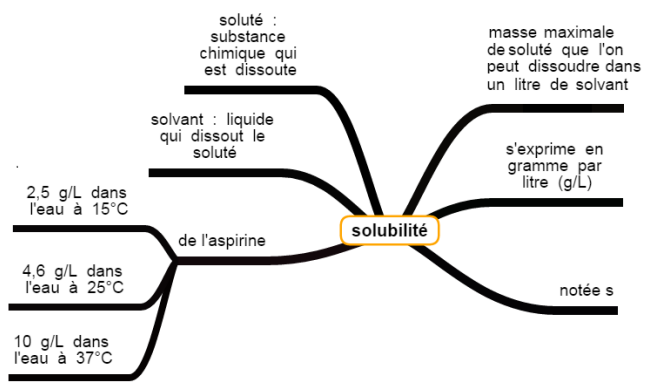
Question 3 : En cas de fièvre, il est recommandé d’ingérer 500 mg d’aspirine, sous la forme d’un comprimé à dissoudre au préalable dans un grand verre d’eau.
Exploiter le document 2 afin de déterminer le volume d’eau minimal nécessaire à la dissolution du comprimé. Commenter le résultat.
On rappelle que la dissolution est le processus par lequel une substance solide ou gazeuse mise au contact d’un liquide passe en solution. Par exemple, la dissolution du sel dans l’eau permet d’obtenir de l’eau salée.
Document 2 : solubilité de l’aspirine
8 éléments
-
1  Organisation et transformation de la matière
Organisation et transformation de la matière
-
2  Organisation et transformation de la matière
Organisation et transformation de la matière
-
3  Organisation et transformation de la matière
Organisation et transformation de la matière
-
4  Organisation et transformation de la matière
Organisation et transformation de la matière
-
5  Organisation et transformation de la matière
Organisation et transformation de la matière
-
6  Organisation et transformation de la matière
Organisation et transformation de la matière
-
7  Organisation et transformation de la matière
Organisation et transformation de la matière
-
8  Organisation et transformation de la matière
Organisation et transformation de la matière
